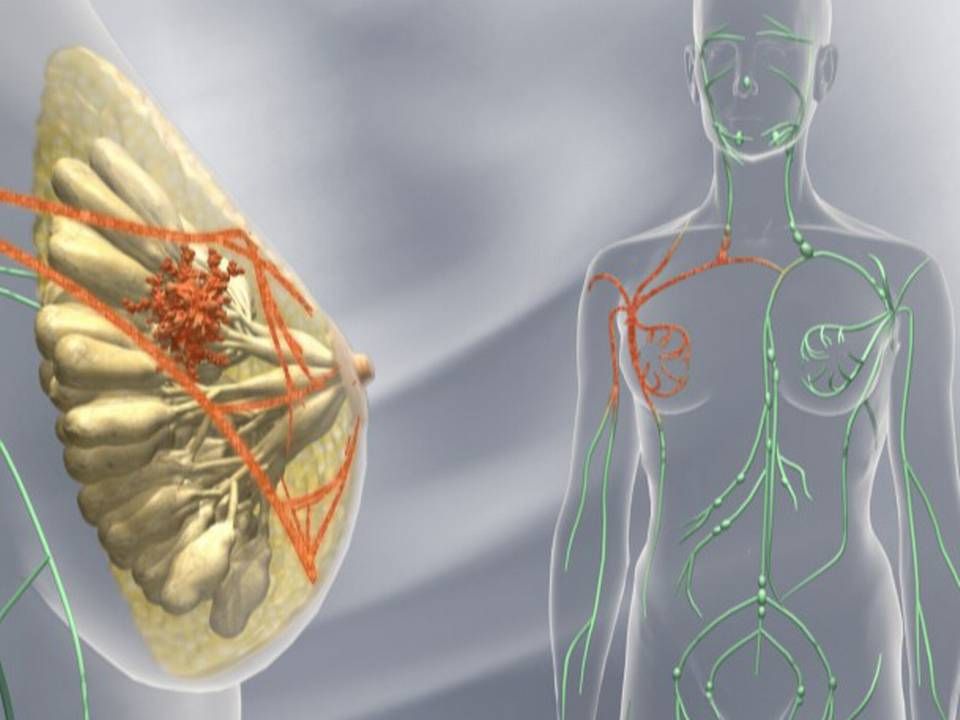
Ny FDA-godkendelse til Roches brystkræftmiddel
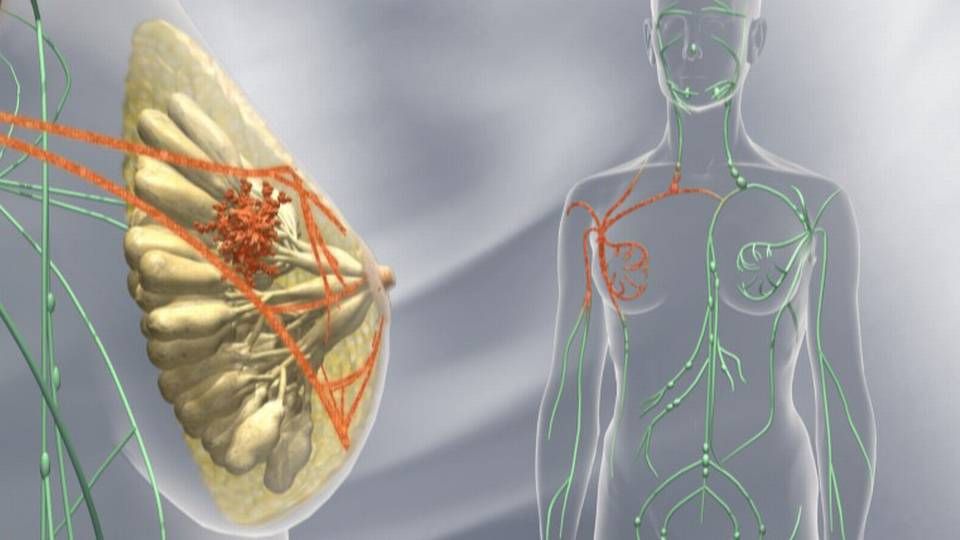
Amerikanske FDA gav i går fremskyndet godkendelse af lægemidlet Perjeta (pertuzumab) fra den schweiziske medicinalkoncern Roche til såkaldt neoadjuverende behandling af brystkræftpatienter – dvs. behandling, som går forud for et kirurgisk indgreb. Det oplyser myndighederne i en pressemeddelelse.
Perjeta blev allerede i 2012 godkendt til behandling af fremskreden metastatisk HER2-positiv brystkræft. I denne type brystkræft har patienterne forøgede mængder af proteinet HER2 i kroppen, hvilket øger kræftcellernes muligheder for at vokse og overleve. Og nu er Perjeta altså også godkendt til de allertidligste stadier af sygdommen.
Lægemidlet skal tages i kombination med kemoterapi-medicin, såsom trastuzumab, inden et kirurgisk indgreb, og i visse tilfælde vil der være behov for opfølgende kemoterapi, oplyser FDA og tilføjer, at Perjeta bliver den første neoadjuverende behandling af brystkræft i USA.
”Vi ser et markant skifte i behandlingsparadigmet for brystkræft i de tidlige stadier. Ved at gøre effektive terapier tilgængelige for udsatte patienter i de tidligste stadier, kan vi måske forsinke eller forebygge tilbagefald,” udtaler Richard Pazdur, som er direktør for Office of Hematology and Oncology Products i FDAs Center for Drug Evaluation and Research, i meddelelsen.
Perjeta markedsføres af den schweiziske medicinalkoncerns datterselskab Genetech i USA. Den nye godkendelse er sket under FDAs specielle Priority Review Program.