Celgenes psoriasismiddel får ny godkendelse

Det amerikanske medicinalselskab Celgene er rykket et skridt nærmere mod at opfylde salgsambitionerne for sit lægemiddel Otezla (apremilast) – et lægemiddel, som man forventer, vil omsætte for op mod 2 mia. dollar på sigt.
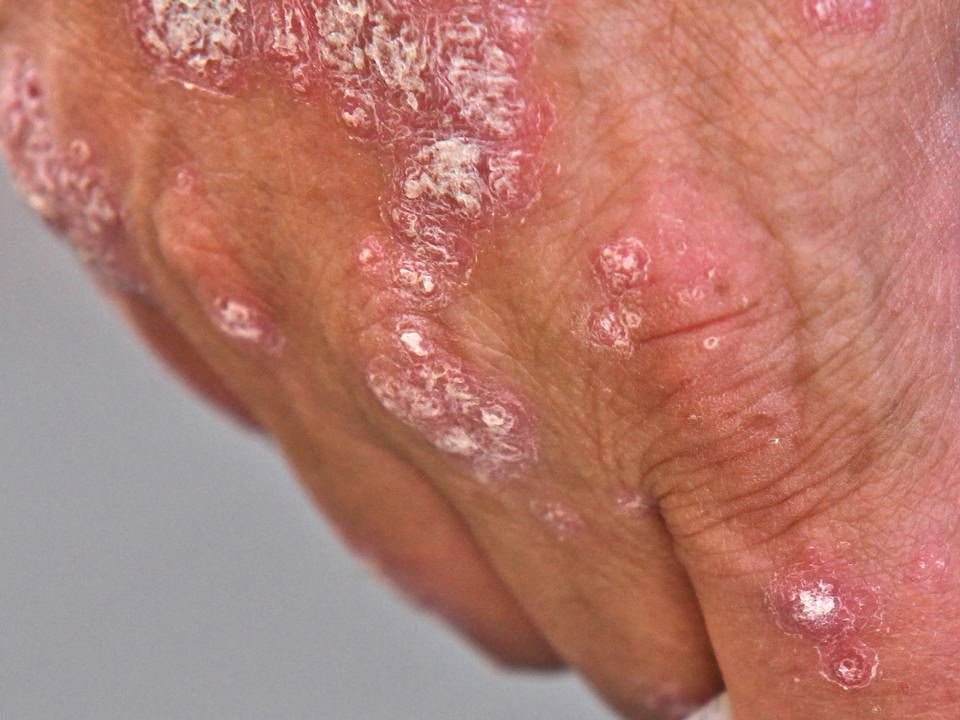
Det står klart, efter at de amerikanske sundhedsmyndigheder, FDA, tirsdag godkendte Otezla i en ny indikation til behandling af patienter med moderat-til-svær plakpsoriasis, der ikke kan afhjælpes af lysbehandling eller systemisk behandling.
Lægemidlet, der er en DPE4-hæmmer i pilleform, er allerede godkendt til behandling af patienter med aktiv psoriasisgigt. Med den nye godkendelse bliver Otezla det første middel af sin slags, der er godkendt i USA til behandling af plakpsoriasis – en sygdom som ifølge selskaber berører mere end 125 millioner mennesker på verdensplan.
Celgene har tidligere meldt ud, at man forventer, at salget af Otezla vil vokse til mellem 1,5 og 2 mia. dollar i 2017, mens de fleste analytikerne ser et noget mere beskedent potentiale i psoriasismedicinen.
Celgenes blockbuster in spe fejler i nicheindikation
Lovende psoriasisdata fra tre selskaber