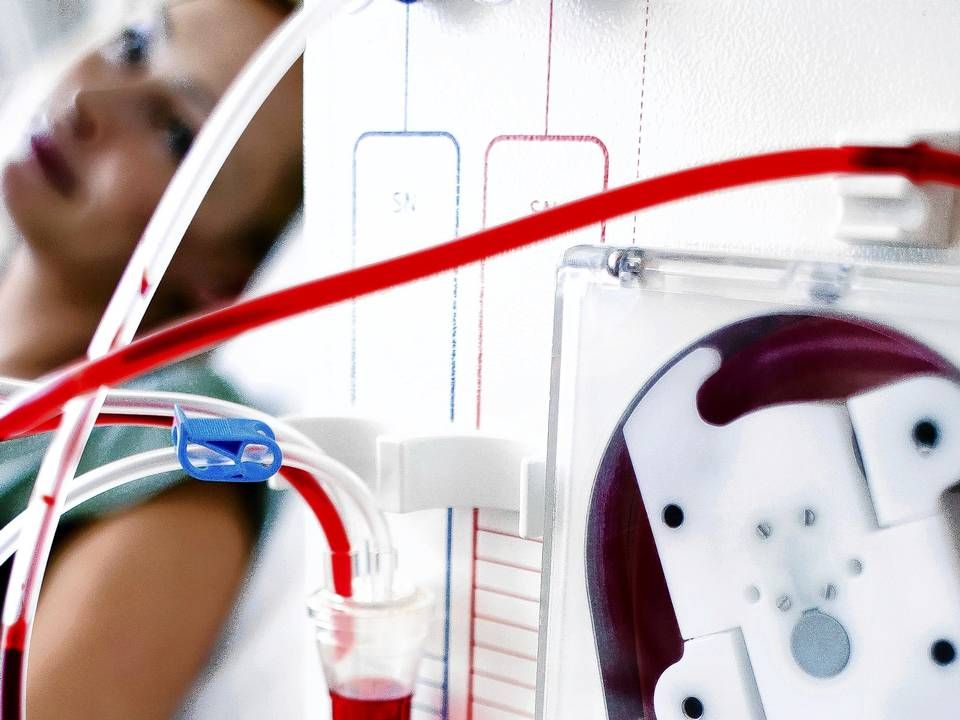
FDA accepterer Veloxis’ ansøgning på nyremiddel
Senest den 7. januar næste år skal de amerikanske lægemiddelmyndigheder, FDA, træffe en afgørelse om, hvorvidt Veloxis’ nyremedicin Envarsus kan bruges til en bredere indikation.
Læs hele artiklen
Få adgang i 14 dage for 0 kr. Det kræver intet kreditkort, og du vil ikke overgå til et betalt abonnement efterfølgende.
Med din prøveperiode får du:
Få fuld adgang til dig og dine kollegaer
Start et gratis virksomhedsprøveabonnementRelaterede artikler
Amerikansk universitet starter studie med Veloxis-middel
For abonnenter