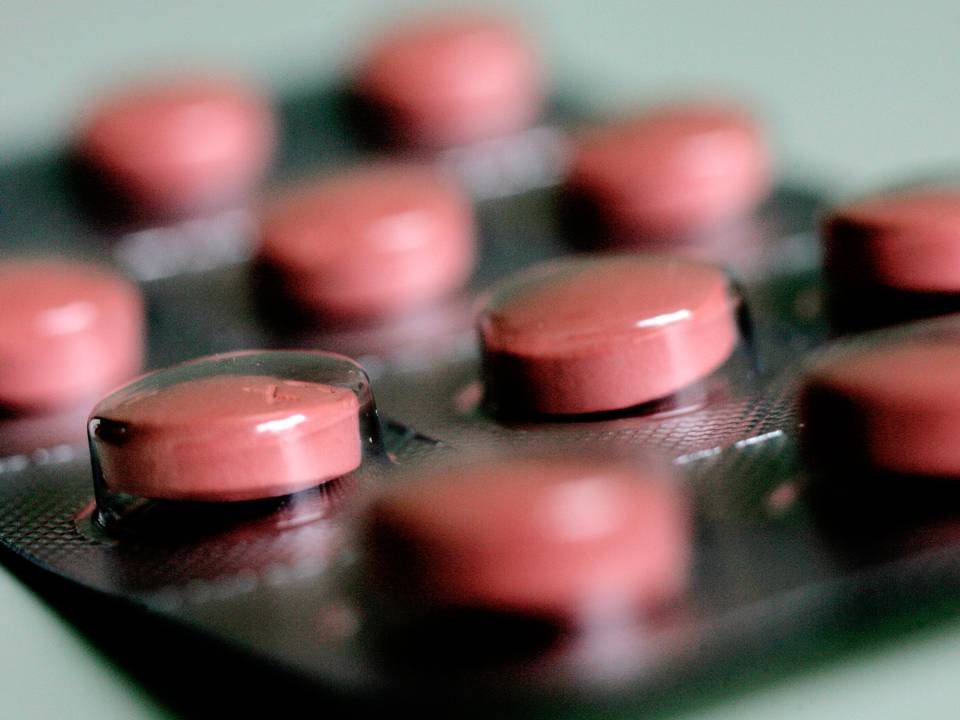
To Teva-midler tilbagekaldt i indsats mod forurenet blodtryksmedicin

Verdens sundhedsmyndigheder har over de seneste uger på stribe tilbagekaldt blodtryksmedicinen valsartan, fordi der er fundet et stof i medicinen, som ikke hører til.
Det gælder også de amerikanske sundhedsmyndigheder, FDA, som blandt andet har tilbagekaldt to generiske versioner af valsartan fra Kåre Schultz' israelske medicinalselskab Teva.
For to uger siden tilbagekaldte den danske lægemiddelstyrelse netop valsartan fra blandt andet parallelimportøren Orifarm.
Det træk blev få dage senere fulgt op af en europæisk tilbagekaldelse fra det europæiske lægemiddelagentur EMA.
Årsagen er, at der er fundet urenheder i de valsartan-produkter, der er produceret af den kinesiske leverandør Zhejiang Huahai Pharmaceutical. Midlerne indeholdt stoffet N-nitrosodimethylamin (NDMA), som ikke hører til i medicinen, og som kan forårsage kræft.
De generiske versioner af valsartan kom på markedet, da patentet på Novartis' Diovan, hvori valsartan er det aktive stof, udløb i 2012.
Inden da solgte Diovan for 36 mia. kr. om året.
Novartis har tidligere sagt til det amerikanske branchemedie Fiercepharma, at Diovan ikke er forurenet og dermed ikke skal tilbagekaldes.
Lægemiddelstyrelsen tilbagekalder blodtryksmedicin fra blandt andet Orifarm